

01
國際藥物工程協會(ISPE)從確保計算機化系統既滿足預定用途又能符合GxP 法規要求出發,組織專家編寫一套簡稱為 GAMP 的方法性指南文件。GAMP指南旨在保障GxP計算機化系統使用中的病人安全、產品質量和數據完整性。它旨在通過以高效和有效的方式在現有的行業良好實踐的基礎上,實現計算機系統適合預定用途并滿足當前的監管要求。該指南從 1995 年第一版開始到 2008 年,已經更新出版了 5 版。
02 GAMP5對系統的軟硬件組件進行分析和歸類。通過分類、風險評估及供應商評估結合起來,為系統確定一個合適的系統生命周期管理策略。 1類:基礎軟件,機房及系統的基礎架構確認; 3類:標準軟件,與設備/儀器相連接的系統補充計算機化系統部分的驗證 4類:可配置軟件,大型網絡版系統(ERP/LIMS)全套計算機化系統驗證文件 5類:定制軟件,代碼審核報告單元測試更嚴格的風險評估
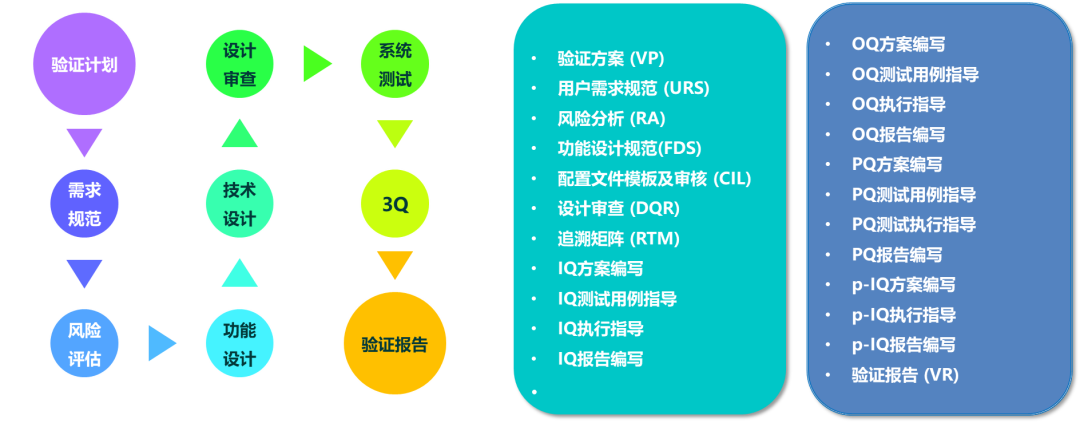
03 醫藥行業的ERP軟件屬于4類,需要按下圖的V模型進行驗證。
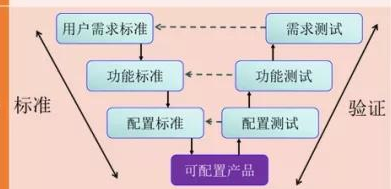
01 生命周期方法 在偏傳統的開發體系下,行業內采用如下的瀑布式軟件開發流程:
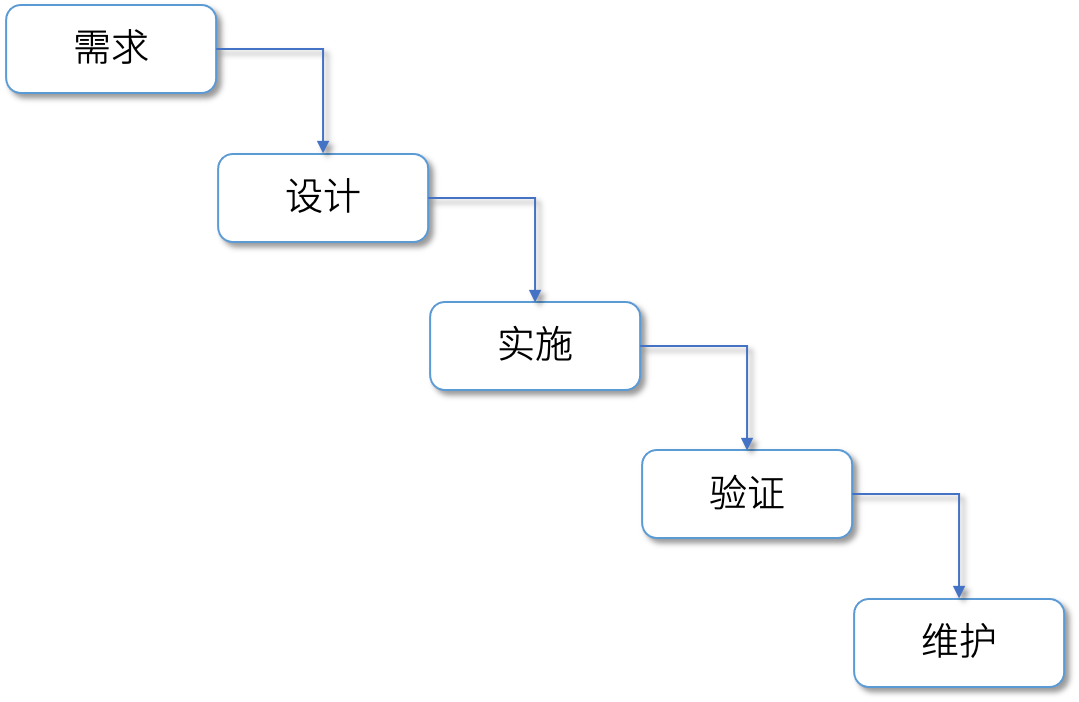
在GAMP5第二版中,迭代和增量模型將配合軟件的敏捷開發方式,達成用戶的期望。
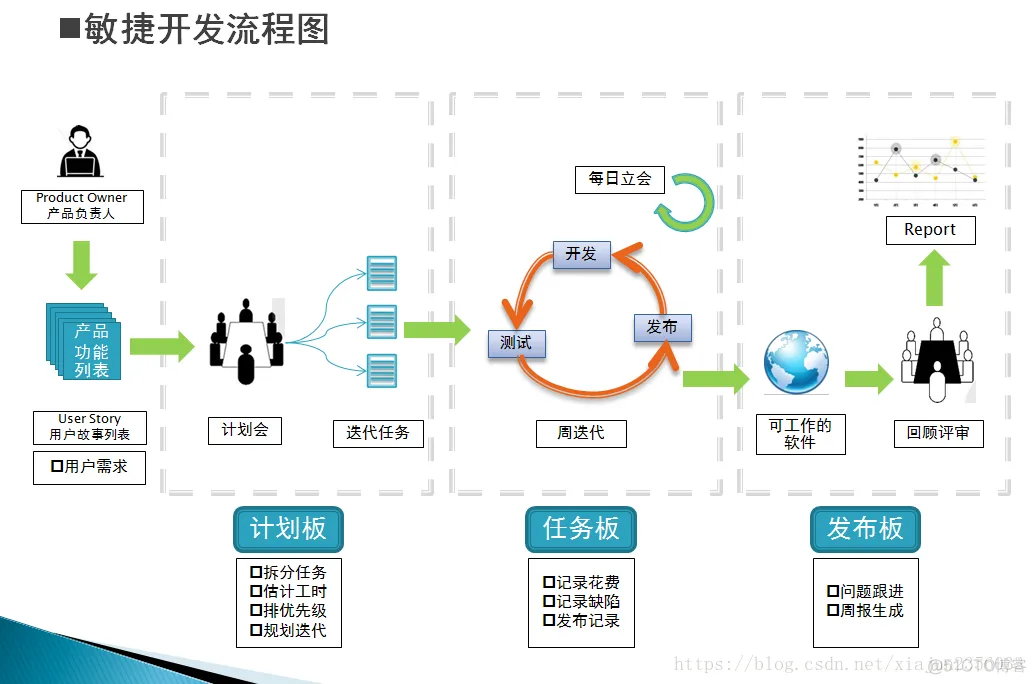
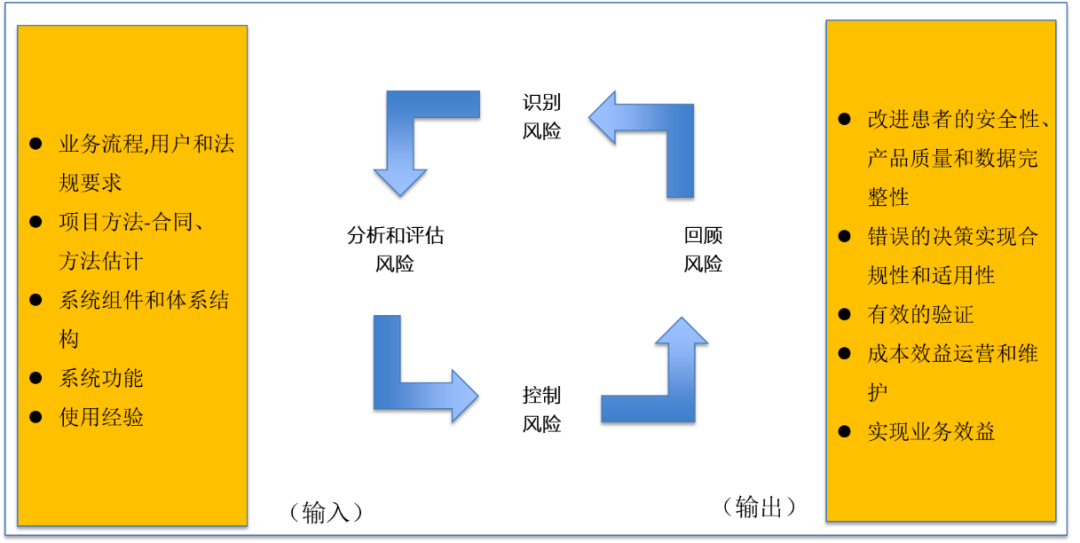
02 基于風險的供應商評估方法 可靠的供應商要具備如下的職能:
步驟 規范 描述 1 建立QMS 供應商應: 1.提供文件化的程序和標準 2.確保各項活動由稱職和受過訓練的員工執行 3.提供符合既定程序和標準的證據 4.啟用并促進持續改進,包括采用當前的軟件方法、良好實踐、以及適當的工具和自動化 2 建立需求 供應商應確保被監管公司定義或提供明確的要求 3 質量計劃 供應商應定義如何對特定產品、應用或服務實施他們的質量管理體系 4 評估次級供應商 作為選擇和質量規劃過程的一部分,供應商應正式評估其次級供應商 5 生產規格 供應商應指定系統以滿足所定義的要求 6 執行設計評審 系統的設計應根據需求、標準和確定的風險進行正式評審,以確保系統將滿足預期的目的,并建立適當的控制以進行管理 7 軟件生產/配置 軟件應根據定義的標準開發,配置應遵循任何定義的規則或建議,并應記錄在案 8 執行測試 供應商應根據批準的測試計劃和測試規范測試系統 9 系統的商業發布 系統向客戶發布應按照正式流程進行 10 提供用戶文檔和培訓 供應商應根據商定的合同提供充分的系統管理文件操作文件和培訓 11 支持和維護運行中的系統 供應商應根據商定的合同支持和維護系統。應充分描述管理和記錄系統更改的過程 12 系統更換和報廢 供應商應根據記錄在案的流程和計劃管理產品/服務的更換或撤銷;供應商還可以根據受監管的公司程序支持注冊公司停用計算機化系統
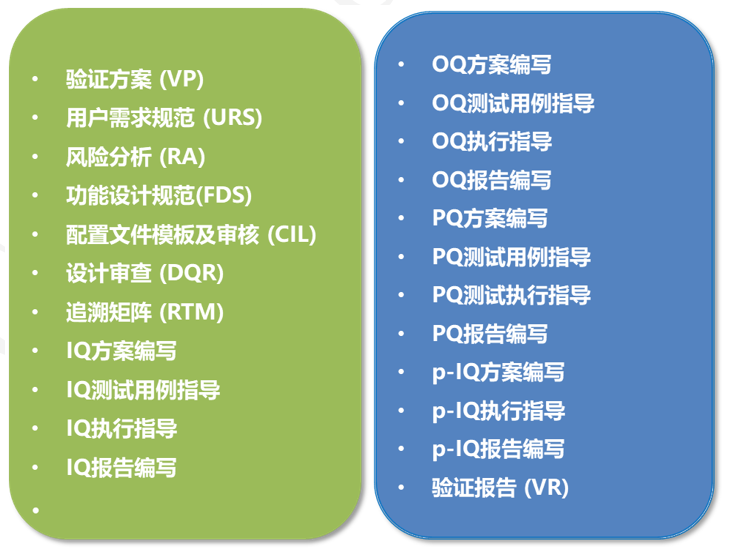
03 項目應基于ISPE-GAMP5的 標準驗證流程及交付物
GAMP5建議的驗證流程如下圖:
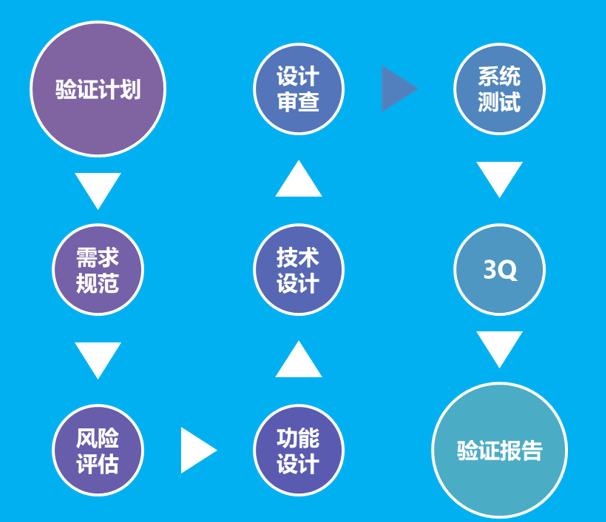
在項目過程中,需要基于以上流程,提供以下的交付物。
04 進行基于風險的測試 進行基于風險的測試,以表明應用軟件在測試環境下按照設計要求運行;進行基于風險的測試,以表明應用軟件在業務流程中按照設計要求運行,具有用于保證系統合規,并符合預定用途的規程。
04 金蝶云·星空醫藥行業合規管理就是基于金蝶云·星空平臺進行開發,無縫融入到金蝶云·星空的標準產品(如供應鏈、生產管理及質量管理等)中,讓金蝶云·星空在滿足醫藥行業通用管理需求時,也滿足醫藥行業的特性要求。

金蝶云·星空醫藥行業解決方案,不但包括行業應用平臺,也提供踐行GMP5的CSV認證服務。
05 ERP系統,是醫藥行業計算機化系統的核心,其主要目的是提高醫藥企業的運營效率和利潤,實現Gxp 合規化管理管理,增強企業的競爭優勢。在GMP5中,所有關于計算機化系統的活動最終在滿足合規要求的同時,也必須具備良好的KPI素養,也就是將效率提升作為重要的衡量指標。
公司地址:上海市浦東新區盛榮路88弄1號樓314室
